(Dieser Artikel erschien zuerst 2004 in „wlb“ und wurde im November 2013 aktualisiert.)
Bei der Entscheidung für die optimale Abluftreinigungsmethode beginnt die Auswahl mit einer Beschreibung der Rahmenbedingungen. Daraus ergeben sich Hinweise, welches Abluftreinigungsverfahren am wirtschaftlichsten wäre. Danach bleibt jedoch noch die Frage zu klären, ob die chemischen Eigenschaften der anfallenden Stoffe das gewählte Verfahren überhaupt zulassen, oder ob mit unliebsamen Überraschungen – etwa Selbstentzündungen, unerwarteten Reaktionen oder ungenügenden Reinigungsleistungen – gerechnet werden muss. Andererseits erlauben es die chemischen Eigenschaften der abzuscheidenden Stoffe manchmal, ein alternatives, günstigeres Verfahren zu wählen.
Zu den am häufigsten eingesetzten Abluftreinigungsverfahren gehören die verschiedenen Arten der Verbrennung, Adsorptions- und Absorptionsverfahren (z. B. Wäscher) sowie biologische Verfahren. Exoten wie Kondensation, Wäsche mit organischen Fluiden oder spezielle Chemisorptionsverfahren führen dagegen ein Nischendasein. Bei partikelbeladenen Abluftströmen kommen zusätzlich verschiedene Arten von Filtern zum Einsatz. Die technischen Randbedingungen, also Volumenstrom, Zusammensetzung und Temperatur des Abluftstromes sind immer die ersten Kriterien bei der Vorauswahl der Abluftreinigungstechnik.
Aber nicht nur die technischen Randbedingungen, auch die chemischen Eigenschaften der abzuscheidenden Stoffe beeinflussen die Einsetzbarkeit der verschiedenen Verfahren.
Vorüberlegungen chemischer Art beim Einsatz von Verbrennungsverfahren
Zwar ist die Verbrennung in ihren verschiedenen Variationen die häufigste in Deutschland installierte Abluftreinigungstechnik, aber die Entscheidung dafür fällt oft als eine Art Negativauswahl. Die Verbrennung erreicht bei geringen oder stark wechselnden Beladungen, bei schwer wasserlöslichen, schwer adsorbierbaren oder wenig bioabbaubaren VOC’s zuverlässig die geforderten Reingaswerte, wo andere Verfahren nicht oder nicht mehr wirtschaftlich einzusetzen sind. Je nach Verfahren – ob katalytisch, thermisch-regenerativ oder nach einer der anderen Varianten – können jedoch die Investitions- und Brennstoffkosten, abhängig von der Anlagengröße, extrem hoch werden, leicht drei- bis viermal so hoch wie etwa bei einem Biofilter
Was muss bei einer Nachverbrennung in Bezug auf die Stoffliste beachtet werden? Wo kann es zu anderen Reaktionsprodukten als Wasser und CO2 kommen?
Halogenierte Verbindungen
Mit halogenierten Verbindungen sind nicht nur Halogenkohlenwasserstoffe gemeint, wie etwa Methylenchlorid oder die meisten Kältemittel, sondern auch Reagenzien wie Chloressigsäure. Abgesehen vom Risiko der Dioxinbildung, welches durch die korrekte Verfahrensführung kontrolliert werden kann, führen halogenierte Verbindungen in einer Verbrennung zur Bildung starker Säuren, welche reingasseitig mit der Zeit zu schwersten Korrosionen führen können, gelegentlich sogar einen nachgeschalteten Wäscher notwendig machen.
Stickstoffhaltige Verbindungen
Stickoxide – Verbindungen der Formel NOx –entstehen bei der Verbrennung von Aminen und anderen stickstoffhaltigen organischen Verbindungen. Die zu erwartende Menge, und somit die Einhaltung der Emissionsgrenzwerte, lässt sich nach folgender Formel abschätzen:
C(NOx) = C(roh)*n*46,01/Mw
Es bedeuten:
- C(NOx) = Konzentration von Stickoxiden auf der Reingasseite, angegeben als NO2 in [mg/Nm³]
- C(roh) = Konzentration (absolut, nicht der C(FID)-Wert!) der stickstoffhaltigen organischen Verbindung im Rohgasstrom in [mg/Nm³]
- n = Anzahl der Stickstoffatome im Molekül
- Mw = Molekulargewicht der stickstoffhaltigen Verbindung.
Bei mehreren verschiedenen stickstoffhaltigen Verbindungen gilt entsprechend:
C(NOx) = Σ{Ci(roh)*ni*46,01/Mwi}
Das Formelresultat ist die Höchstmenge an NO2, die aus der Verbrennung der stickstoffhaltigen Verbindungen entstehen kann, die Menge kann aber, abhängig von den Randbedingungen der Verbrennung, auch geringer sein.
Katalysatorgifte
Bei der katalytischen Nachverbrennung (KNV) ist die größte Sorge, das Vergiften des Katalysators auszuschließen, da er meist nicht regeneriert werden kann. Aufgrund der Verschiedenartigkeit der Katalysatoren wird hier als Daumenregel nur angegeben, dass sich Phosphor-, Schwefel- und Halogenhaltige Verbindungen nicht für Edelmetall-Katalysatoren eignen. Da man die Katalysatorgifte nur auf Grund von langwierigen Versuchsreihen oder aber bitteren Erfahrungen herausfindet, wird die Liste der für das Verfahren geeigneten Verbindungen ziemlich restriktiv gehandhabt. Alkohole, niedermolekulare Ester und Ketone sind gute Kandidaten für eine KNV. In den letzten Jahren sind allerdings eine Reihe von Metalloxidkatalysatoren auf dem Markt erschienen, welche im Vergleich zu Edelmetallkatalysatoren zwar selektiver in der Wirkung, dafür aber gegen einzelne Katalysatorgifte beständig sind.
Chemie im Abfall
In den Luftkanälen auf der Rohgasseite sind nur bei höheren Konzentrationen – etwa wenn Brüden abgesaugt werden – Reaktionen zu erwarten. Dann kann es sogar zu einer Diffusion einzelner Stoffe gegen die Strömungsrichtung und Bildung von Ablagerungen kommen. Bei kleineren Beladungen und höheren Strömungsgeschwindigkeiten verschwindet dieser Effekt oder ist nur bei sehr starker Triebkraft der Reaktion, z. B. H2O und HCl, zu beobachten.
Anders hingegen in Pumpensümpfen und Absetzgefäßen, in denen die organischen Verbindungen – meistens bei Anwesenheit von Wasser – über längere Zeit bei Raumtemperatur oder darüber lagern: Dort kann sich auch bei geringerer Reaktivität (etwa bei Alkoholen, Estern) eine Reihe von Reaktionen abspielen, meistens Oxidationsreaktionen und Hydrolysen. Oft führen diese zu Säuren. Die Kondensate haben dann korrosive Eigenschaften, welche aus der Stoffliste der verwendeten Lösungsmittel nicht direkt hervorgehen. Halogenkohlenwasserstoffe können jedoch aus organischen Lösungsmitteln und salzhaltigen (also halogenidhaltigen) Wässern unter diesen Bedingungen nicht entstehen.
Kondensationsanlagen
Die Kondensation wird meist erwogen, wenn ein flüchtiger Stoff wiedergewonnen werden soll. Dies ist zwar auch auf dem Weg der Adsorption/Desorption möglich, allerdings bewirken die zur Desorption nötigen erhöhten Temperaturen, dass thermisch weniger stabile Stoffe (so wie die meisten Monomeren oder verzweigtkettigen Alkohole) über eine Kondensation wiedergewonnen werden müssen, weil sie sich bei der Desorption von Kohle oder Zeolith zersetzen würden. Diese Zersetzung betrifft zwar nicht das gesamte Lösungsmittel, aber das verunreinigte Regenerat entspricht oft nicht mehr den Anforderungen und kann ohne Aufbereitung nicht rückgeführt werden. Dies wiederum ist in den meisten Fällen, im Vergleich zu neuer Ware, nicht rentabel.
Das große ökonomische Hindernis bei der Kondensation als Stand-alone-Abluftreinigungsverfahren sind die tiefen Temperaturen, welche erreicht werden müssen, zur Einhaltung der VOC-Richtlinie z. B für Dichlormethan weit unter – 100 °C, für Methanol ca. – 80 °C. Daher lohnt sich dies Verfahren nur in Ausnahmefällen, etwa bei der Behandlung recht konzentrierter Ströme eher hochsiedender Stoffe.
Gemische und ihre Tücken
Bei Vorhandensein eines Gemisches verschiedener Lösungsmittel kann der Dampfdruck des Kondensates – bei Vorliegen der Dampfdruckkurven der einzelnen Komponenten – grob nach dem Raoult’schen Gesetz bestimmt werden. Nach dem Raoult’schen Gesetz ist der Dampfdruck p(ges) einer Mischung gleich der Summe der Partialdrücke pi. Die Partialdrücke wiederum sind die Produkte aus dem Dampfdruck der Komponente i und ihrem Molenbruch Xi in der Mischung.

Raoult’sches Gesetz, Abschätzung von Mischungsdampfdrücken
Dies ist nur bei den „idealen Mischungen“ der Fall.
In der Realität werden jedoch fast immer Mischungseffekte auftreten, wie Dampfdruckerhöhungen, -erniedrigungen oder azeotropes Verhalten. Die Mischungseffekte können bei chemisch nicht ähnlichen Verbindungen erheblich werden, jedoch wird man die Daten für solche Gemische nur selten zur Verfügung haben. Eine Literatur- bzw. Datenbankenrecherche kann sie bei Standardlösungsmitteln oft zu Tage fördern. Dabei darf man jedoch das stets anwesende Wasser nicht vergessen: Handelt es sich bei der Abluft um verunreinigte Atmosphärenluft, wird diese um 11 g Wasser/Nm³ enthalten – eine signifikante Menge gegenüber der organischen Beladung, die meist nur im einstelligen Gramm-Bereich liegt. Toluol bildet mit Wasser ein Azeotrop, Benzol mit Wasser ebenfalls. Die Abschätzung nach dem Raoult’schen Gesetz würde bei Anwesenheit von Wasser nicht einmal annähernd zutreffen.
Chemie im Kondensat
Reaktionen im Kondensat, auch Polymerisationen und Hydrolysen, sind zunächst unwahrscheinlich. Das liegt erstens an der tiefen Kondensationstemperatur, zweitens muss der Gasstrom vor der Tieftemperaturkondensation ohnehin vom Wasser weitestgehend befreit werden. Es ist aber empfehlenswert, gerade Monomere nicht zu lange in einem sich erwärmenden Kondensatsammler stehen zu lassen (womöglich tage- oder wochenlang), sondern so schnell wie möglich weiterzuverarbeiten.
Bei der Kondensation des Wassers werden je nach Rohgaszusammensetzung auch schon große Mengen organischer Lösungsmittel mitkondensiert. Dabei kann es im Absetzgefäß zu der gewünschten Phasentrennung kommen, diese kann aber auch ausbleiben. Die Voraussage ist schwierig, wenn eine Mischung von Wasser, wasserlöslichen und unlöslichen Komponenten kondensiert werden soll. Vorversuche im Labor (anhand von reinen Lösungsmitteln, welche bei Raumtemperatur gemischt wurden) führen gelegentlich zu einem falsch-positiven Ergebnis, weil Verunreinigungen und daraus resultierende Emulsionen sowie Aufschäumen, etwa durch Druckwechsel, eine große Rolle für die Phasentrennung spielen.
Die Chemie der Wäscher
Problemfälle, die weniger leicht beurteilt werden können als die etablierten Standardanwendungen für Wäscher, liegen vor, wenn VOC’s (mit) ausgewaschen werden sollen.
Während Methanol, Ethanol, 1-Propanol mit Wasser unbegrenzt mischbar sind, bildet Wasser mit 1-Butanol, Dichlormethan oder Toluol zwei Phasen. Die Bildung von zwei Phasen bedeutet aber nicht, dass das entsprechende Lösungsmittel in Wasser unlöslich ist: 0,52 g Toluol lösen sich in 1 l Wasser, Dichlormethan ist zu 20 g/l in Wasser löslich, 1-Butanol sogar zu 79 g/l (bei 20 °C). Kann man diese nicht wassermischbaren Substanzen also doch mit Wasser auswaschen? Diese Frage wird besonders wichtig, wenn bestimmte Komponenten des Abluftstromes ohnehin einen Wäscher erforderlich machen, und es darum geht herauszufinden, ob a) eine Nachbehandlungsstufe erforderlich ist oder nicht und b) wie der Wasserverbrauch beeinflusst werden wird.
Von entscheidender Bedeutung ist der Dampfdruck der gelösten VOC’s im Waschwasser. Bei einer einzelnen schwer löslichen und relativ flüchtigen Verbindung, wie Styrol oder Toluol, kann zur Abschätzung der minimal benötigten Wassermenge pro Stunde bei einem geforderten Reingaswert von 50 mg/m³, Normaldruck und T = 20 °C die folgende Formel angewendet werden (man beachte aber, dass die vom Henry-Gesetz abgeleitete Formel bei besser löslichen oder wassermischbaren Stoffen aufgrund der höheren Arbeitskonzentrationen keine Anwendung finden kann):
dm(Wasser)/dt={(dV/dt)*CA(roh)}/{kHΘ*1,12*10-3}
Es bedeuten:
- dm(Wasser)/dt: Wassermenge in [kg/h], welche zur Aufbereitung (Strippen, Oxidation o. ä.) oder Entsorgung abgeführt werden muss
- dV/dt: Volumenstrom Rohgas, in [m³/h]
- CA(roh) : Beladung von A im Rohgas, in [g/m³]
- kHΘ : Henry-Konstante (als Löslichkeit, nicht als Fugazität), in [mol/l*atm]
Das Verhalten von Lösungsmittelgemischen bei der Abluftwäsche hängt vom Einzelfall ab. Einzelne Komponenten könnten die Löslichkeit für andere verringern oder erhöhen. Sind zum Beispiel salzhaltige Stäube in der Abluft, wird die Wasserlöslichkeit organischer Verbindungen dadurch gesenkt. Dagegen kann ein wassermischbares Lösungsmittel (z. B. Ethanol) die Wasserlöslichkeit einer eigentlich nicht wasserlösichen organischen Verbindung (etwa Toluol) signifikant erhöhen. Von den vorhandenen Stoffen hängt es auch ab, wie das Waschwasser behandelt werden kann – chemisch oder physikalisch, also z. B. durch Oxidationsmittelzusatz oder z. B. durch Strippen und Kondensation.
Sonderfall PEG-Wäscher
Für nicht wasserlösliche Verbindungen, die nach anderen Verfahren nicht abscheidbar sind, hat sich die Wäsche mit einem organischen, wenig flüchtigen Polyethylenglykolderivat (PEG-DAE) bewährt. Die erreichbaren Reingaswerte sind gut, jedoch sind Investitions- und Energiekosten sehr hoch, da die Waschflüssigkeit allein durch eine Vakuumdestillation wieder regeneriert werden kann, und diese Regeneration außerdem in den meisten Fällen kontinuierlich erfolgen muss, einschließlich Ein- und Ausschleusung der Waschflüssigkeit in die Destillation.. Der PEG-DAE ist chemisch recht beständig, jedoch sollte die Verträglichkeit der abzuscheidenden Stoffe mit der Waschflüssigkeit – es gibt von dieser mehrere Varianten – vorher geprüft werden. Eventuell wird es notwendig, eine wässrige Waschstufe und eine Wasserabscheidung vorzuschalten (Polyglykole sind stark hygroskopisch).
Adsorptionsanlagen – chemische Vorüberlegungen
Bei geeigneten Adsorbtiv-Adsorbens-Kombinationen bleiben die Reingaswerte, unabhängig von der Rohgaskonzentration, bis zum Durchbruchspunkt relativ konstant. Adsorptionsanlagen eignen sich daher besonders, wenn gering oder wechselnd beladene Gasströme bzw. solche, die nur zu wenigen Stunden am Tag auftreten, behandelt werden sollen, es sind aber auch viele kontinuierlich arbeitende Anlagen realisiert worden. Etwa bei stark verdünnten, halogenkohlenwasserstoffhaltigen Rohgasströmen, die weder auskondensiert noch verbrannt noch gewaschen werden können, ist die Adsorption das Verfahren der Wahl.
Adsorptionsanlagen, die zur in situ-Regeneration ausgelegt sind, gestatten zudem auch die Rückgewinnung des Adsorptivs.
Auf der anderen Seite kann eine Adsorptionsanlage zu einem Problemfall werden: Wenn die Reingaswerte nicht eingehalten werden, oder wenn es gar zu einer Selbstentzündung des Adsorbates kommt – manchmal mit katastrophalen Folgen.
Welche Adsorbenzien stehen zur Verfügung, welche Stoffe können damit adsorbiert werden? In welchen Fällen kann es zur Selbstentzündung kommen?
Das am häufigsten verwendete Adsorbens ist Aktivkohle. Ebenfalls sehr häufig verwendet werden synthetische, hydrophobe Zeolithe. Für spezielle Fälle stehen reaktiv imprägnierte Adsorbenzien – meistens ebenfalls auf Kohle- oder Zeolithbasis – zur Verfügung.

Verschiedene Adsorbenzien: Zeolith zur Wasseradsorption, Aktivkohle, eine Mischung zweier hydrophober Zeolithe und „Envisorb“, eine Mischung von Aktivkohle und Silicagel.
Aktivkohle kann ein besonders breites Spektrum an Verbindungen adsorbieren und ist das vielseitigste aller Adsorptionsmittel, welches sich durch Modifikationen in der Herstellprozedur fast beliebig variieren lässt. Auch Molekularsiebe – (semi)synthetische oder natürliche Zeolithe – gibt es in sehr vielen Strukturtypen, welche sich untereinander im Verhalten noch stärker unterscheiden als die Aktivkohlen.
Selbstentzündung von Festbettadsorbern
Die Brennbarkeit der Aktivkohle birgt ein gewisses Risikopotenzial. Molekularsieb als solches ist nicht brennbar, das bedeutet aber nicht, dass es – mit organischen Molekülen belegt – nicht dennoch aufflammen kann. Die Selbstentzündung von Adsorbaten hat zwei zusammenwirkende Ursachen: erstens die Exothermie des Adsorptionsvorganges und zweitens die Aktivierung (und somit Erniedrigung des Flammpunktesr Zündtemperatur) des adsorbierten Moleküls. Ist freier oder adsorbierter Sauerstoff vorhanden, kann im Adsorbat eine langsame Oxidationsreaktion ihren Anfang nehmen. Wird die dabei entstehende Reaktionswärme nicht genügend abgeführt, können sich in der Schüttung Hitzenester (sogenannte Hotsports) bilden, die unter bestimmten Umständen zu einer Selbstentzündung der Schüttung führen. Im Zusammenhang mit Aktivkohle haben sich z. B. trocknende Öle oder oxidierende Verbindungen als besonders kritisch erwiesen, ebenso einige Amine; bei Zeolithen – bei denen solche Ereignisse selten vorkommen – sind einige Selbstentzündungen im Zusammenhang mit schwefelorganischen und verschiedenen anderen Verbindungen bekannt geworden.
Inerte Verhältnisse verhindern die Selbstentzündung, allerdings nicht bei Anwesenheit von oxidierenden Verbindungen. Weitere Schutzmaßnahmen neben einer sorgfältigen Auswahl der Adsorbtiv-Adsorbens-Kombination sind ausschließlich verfahrenstechnischer Art und betreffen die Luftführung sowie spezielle Einbauten, etwa Deflagratoren.
Adsorbensauswahl
Die optimale Auswahl eines Adsorbens ist – vor allem bei einem zu adsorbierenden Vielstoffgemisch – eine komplexe Fragestellung. Man ist auf Daten zur chemischen Beständigkeit und auf Adsorptionsisothermen für das spezielle Adsorbens angewiesen, wobei sorgfältig geprüft werden sollte, auf welche Weise diese gemessen wurden. Extrapolationen innerhalb einer Stoffgruppe – also z. B. von einem Halogenkohlenwasserstoff auf den nächsten zu schließen – sind immer problematisch. Einige Isothermenvergleiche innerhalb von Stoffgruppen habe ich auf meiner Website zusammengestellt.
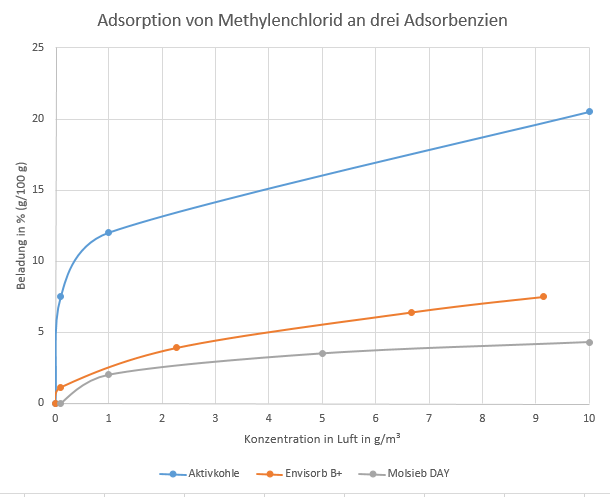
Adsorption von Methylenchlorid an drei verschiedenen Adsorbenzien
Adsorbierte Stoffe können sich auch gegenseitig beeinflussen, wie in vielen Veröffentlichungen bereits gezeigt wurde.
Da die Regeneration eines Zeolithadsorbens in der Praxis der Abluftreinigung nicht ohne Temperaturerhöhung auskommt – auch bei Druckwechseldesorption nicht – können thermisch instabile Stoffe nicht nach einem solchen Verfahren weder abgereinigt noch wiedergewonnen werden. Das Desorbat enthält in solchen Fällen immer Zersetzungsprodukte. Problematischer noch ist, dass solche zersetzlichen Stoffe zu vermehrtem Fouling des Adsorbens führen, d. h. verkokte Rückstände verbleiben auf dem Molekularsieb und belegen dessen innere Oberfläche. Das Adsorbens kann dann nur durch eine Grundregeneration, welche in situ nicht ausgeführt werden kann, wieder gebrauchsfähig gemacht werden. Die Rückstände selbst erhöhen das Gefahrenpotenzial einer Selbstentzündung – einfach, weil mehr Brennstoff vorhanden ist.
Biofilter
Obwohl Biologische Abluftreinigungsanlagen verschiedenster Bauart gezeigt haben, dass auch als „mäßig bis schwer abbaubar“ einzustufende Stoffe aus der Luft abgereichert werden können, gibt es doch Chemikalien, für die dieses Verfahren nicht empfohlen werden kann. Alles was mikrobizid, bakteriostatisch, desinfizierend, antibiotisch oder sonst wie den Bakterienstoffwechsel hemmend ist, kann mit diesem Verfahren nicht auf Dauer behandelt werden.
Besonders geeignet ist der Biofilter, wenn es darum geht, Gerüche zu mildern, etwa bei der Abluft aus der Verarbeitung tierischer und pflanzlicher Rohstoffe. Oft wird die Kohlenstofffracht des Reingases im Vergleich zum Rohgas nicht signifikant vermindert, da kein vollständiger Abbau zu CO2 und Wasser stattfindet. Dies spielt bei einer reinen Geruchsbeseitigung aber keine Rolle.
Sonderfälle
Für mit Partikeln beladene Abluftströme (Stäube oder Aerosole), falls sie nicht ohnehin mit einem Wäscher mitbehandelt werden, kommen verschiedene Arten von Filtern zum Einsatz. Partikelfilter werden nach Teilchengröße und chemischer Natur der aufzufangenden Teilchen ausgewählt. Elektrofilter können oft noch bessere Abscheidungsgrade erzielen als mechanische Filter, jedoch unterliegen sie gewissen Einschränkungen. Diese betreffen die Ablufttemperatur, den Flammpunkt der abzuscheidenden Stoffe, deren Neigung zur Belagbildung etc. Dieses sollte bei dem Versuch, einen Elektrofilter in „unerprobtem Terrain“ einzusetzen, bedacht werden.
Bei geringen Mengen an abzuscheidender Substanz kann auch eine Adsorptionsanlage mit Einweg-Adsorbens zur Anwendung kommen, am häufigsten wird das Aktivkohle sein. Für manche Substanzen können katalytisch oder mit Oxidationsmitteln beschichtete Adsorbenzien zum Einsatz kommen, die den adsorbierten Schadstoff zersetzen und auch bei geringer Adsorptionsneigung des Schadstoffes zu guten Reingaswerten führen.
Bei leicht oxidierbaren Substanzen kann auch eine UV/Katalysatoranlage zum Einsatz kommen. Sie funktioniert durch die laufende Entstehung von Hydroxylradikalen in der feuchten Gasphase unter UV-Bestrahlung. Ein Katalysator unterstützt die Umsetzung der abzubauenden Substanzen mit den Hydroxylradikalen. Auch dieses Verfahren führt – je nach abzubauender Substanz – nicht immer zu CO2 und H2O, sondern zu größeren Molekülfragmenten und somit auch nicht zu niedrigeren C(FID)-Werten in der Abluft. Jedoch können Gerüche mit solchen Verfahren oft gut beseitigt werden.
Fazit
Genaue Betrachtung der chemischen Eigenschaften abzuscheidender Stoffe erleichtert die Planung einer Abluftreinigungsanlage in mehreren Punkten: Bei den Vorversuchen, weil manches schon im Vorfeld theoretisch geklärt werden kann, und weil nicht aussagekräftige Versuche vermieden werden. Bei der Planung, weil das optimale Verfahren mit größerer Sicherheit ausgewählt werden kann. Und auch für die Erstellung einer Sicherheitsbetrachtung ist die Kenntnis der chemischen Eigenschaften der beteiligten Stoffe unbedingt vonnöten.
Nico meint
Mir war nicht klar, dass Elektrofilter noch besser filtern, als chemische Filter. Die Fakten und Infos hierzu sind sehr interessant. Dann werde ich wohl wieder mehr mit Elektrofiltern arbeiten.
Claudia Arnold meint
Als mechanische Filter, steht in dem Artikel, aber es kommt absolut auf die Form und die Substanz in der Abluft an. Für Stoffe mit Flammpunkt unter 60 °C oder für zu feine Aerosole (bzw. gar keine, also VOC) kann man keine Elektrofilter verwenden. Perfekt sind sie dagegen für Stäube oder Aerosole, die einerseits die Sicherheitskriterien erfüllen und die außerdem dazu neigen, die (deutlich einfacheren und günstigeren) mechanischen Filter zuzusetzen.