Glossar
- Nitrifikation: Umwandlung von Ammoniak NH3 zu Nitrat NO3– durch Mikroorganismen.
- Denitrifikation: Umwandlung von Nitrat NO3– nicht zu Ammoniak, sondern zu Stickstoff N2 und Stickoxiden wie Stickstoffmonoxid NO und Lachgas N2O.
- EU „Nitratrichtlinie„: Richtlinie 91/676/EWG, die durch Einführung guter Düngerpraxis eine Überdüngung mit Nitraten verringern sollte. Diese wurde in Deutschland 1996 durch die Einführung der 2012 novellierten, aber (nach Meinung vieler) immer noch nicht ausreichenden Düngeverordnung umgesetzt.
Der Anlass
Ich denke, ich sollte meine google Alerts abmelden, denn zum Schlagwort „zeolite“ spülen sie mir wenig Sinnvolles in den Posteingang. Vor einigen Wochen war zum Beispiel ein Hinweis auf den folgenden Artikel dabei: „EU-Richtlinie wegen Nitratwerte: ZEO Grow – natürlicher Zusatz für Dünger und Gülle- mit aktivem Grundwasserschutz„. Die Überschrift finde ich etwas irreführend und der Artikel tut wenig zur Aufklärung, daher möchte ich hier die Hintergründe etwas beleuchten.
1. Nitrat wird von Klinoptilolith nicht zurückgehalten
Ammonium (weniger das freie Ammoniak) wird von Zeolithen, auch Klinoptilolith, in gewisser Menge zurückgehalten. Nitrat NO3– dagegen ist ein Anion, und wenn dieses gebunden werden soll, muss der Zeolith chemisch vorbehandelt werden. Man macht dies mit oberflächenaktiven Substanzen.
Ein mit diesen Substanzen getränkter Zeolith ist selbstverständlich kein „natürliches Mineral“ mehr. Ich bin keine Expertin für diese Art von Rechtsfragen, bezweifle aber, dass man derlei Material auf landwirtschaftlichen Flächen ausbringen darf. Außerdem ist der so vorbehandelte Zeolith auch (a) deutlich teurer und (b) nicht im Handel zu haben, sondern Material, das zu Forschungszwecken in kleineren Mengen hergestellt wurde. (Literatur: [1] – [6])
Mit Phosphat bzw. Arsenat und Klinoptilolith hat man schon eher Erfolg: Der Effekt beruht auf dem Calciumanteil mancher Klinoptilolithe, die mit Phosphat- und Arsenat-Anionen unlösliche Salze bilden. Diese fallen irgendwo in den Ritzen und Spalten des Minerals aus (vielleicht sogar zum Teil im Porensystem) und sind dann nicht mehr mobil. Das bedeutet, die Pflanzen können diese Ionen nicht mehr resorbieren, und die Ionen können auch nicht mehr ins Grundwasser auslaugen (z. B. [7]). Mit Nitrat jedoch, das keine unlöslichen Salze bildet, lässt sich eine Immobilisierung nicht erreichen.
2. Um was geht es also wirklich?
Die Umwandlung von Nitrat zu Stickstoff und Stickoxiden wird als „Denitrifikation“ bezeichnet. Nitrat ist als pflanzenverfügbare Form von Stickstoff eigentlich wünschenswert, aber ein Überschuss ist schädlich. Stickstoff ist harmlos – ca. 80% unserer Atmosphäre sind Stickstoff – aber Stickoxide wie Stickstoffmonoxid und Lachgas sind Treibhausgase. Dennoch ist dies ein Weg zur Reduktion von überreichlich eingetragenem Nitrat, um der Überdüngung vorzubeugen.
Die Denitrifikation wird von Mikroorganismen besorgt, und die porösen Zeolithe mit ihren austauschbaren Ionen können gut als Träger solcher Biofilme fungieren [8]. Eine Zugabe von Zeolith zu einer Denitrifikation, sowohl in Lösung (Kläranlage) oder in Böden (Acker) kann die Denitrifikation beschleunigen und so effektiv den Nitratgehalt senken.
Was aber nicht funktioniert: Große Mengen überschüssiges Nitrat zurückzuhalten, bis die Mikroorganismen die Denitrifikation beendet haben.
Der umgekehrte Fall
Das Gegenstück zur Denitrifikation ist die Nitrifikation: Hier wird Ammoniak bzw. Ammonium in Nitrat umgewandelt, ebenfalls mikrobiologisch.
Stickstoff aus Exkrementen – Jauche, Gülle, Mist etc. – fällt zunächst in der Form von Harnstoff an und wird vom Enzym Urease (z. B. aus Bakterien) zu Ammoniak NH3 umgesetzt. Bei mild sauren pH-Werten liegt der größte Teil als Ammonium NH4+ vor, steht aber immer noch mit Ammoniak im Gleichgewicht. Ammoniak ist ein Gas, es verflüchtigt sich also, vor allem bei Wärme und Sonne, und der Ammoniumstickstoff ist somit nicht mehr im Boden, sondern in der Atmosphäre, wo er höchst unerwünscht ist.
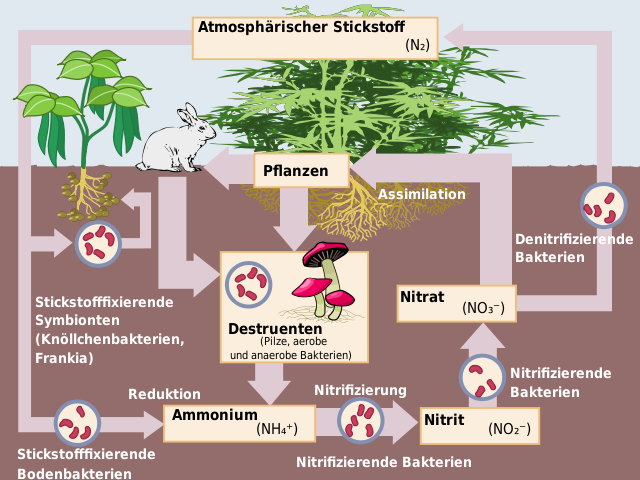
Nitrifikation verwandelt den Ammoniumsticktoff in Nitratstickstoff und schließt somit den Stickstoffkreislauf. So wird Stickstoff aus tierischen Quellen für die Pflanzen verfügbar gemacht, und auch hierbei kann Zeolith eine hilfreiche Beigabe sein. Zeolithe können Ammonium sogar in gewissen Mengen zwischenspeichern, bis die Nitrifikation im außen aufliegenden Biofilm abgeschlossen ist. Dieser Effekt wird in großem Umfang in der Aquakultur ausgenützt, die zu einem der größten Verbraucher von natürlichen Zeolithiten geworden ist, dank des Riesenappetits der Menschheit auf Krabben und Fisch (siehe z. B. [9], [10]). Aber auch für Lebenserhaltungssysteme etwa in der Raumfahrt überlegt man die Anwendung [11].
Etwas mehr über die komplizierte Beziehung zwischen Zeolithen und Ammoniak steht in den Blogbeiträgen „Modifizierung von Naturzeolithen…“ und „Zeolithe zur Geruchsbekämpfung„.
[1] Miazga-Rodriguez, M. et al. Enhancing nitrification at low temperature with zeolite in a mining operations retention pond. Front Microbiol 3, 271 (2012).)
[2] Lin, J. W., Zhu, Z. L., Zhao, J. F., Zhang, H. H. & Zhan, Y. H. [Efficiency and mechanics of surfactant modified zeolite with nitrate adsorbed to control nitrogen and phosphorus release from sediments].
[3] Guan, H. et al. Variation in performance of surfactant loading and resulting nitrate removal among four selected natural zeolites. J Hazard Mater (2010). doi:S0304-3894(10)00954-4 [pii] 10.1016/j.jhazmat.2010.07.069
[4] Zhan, Y., Lin, J. & Zhu, Z. Removal of nitrate from aqueous solution using cetylpyridinium bromide (CPB) modified zeolite as adsorbent. J Hazard Mater 186, 1972–1978 (2011).
[5] Bhardwaj, D., Sharma, M., Sharma, P. & Tomar, R. Synthesis and surfactant modification of clinoptilolite and montmorillonite for the removal of nitrate and preparation of slow release nitrogen fertilizer. J Hazard Mater 227–228, 292–300 (2012).
[6] Malekian, R., Abedi-Koupai, J. & Eslamian, S. S. Influences of clinoptilolite and surfactant-modified clinoptilolite zeolite on nitrate leaching and plant growth. J Hazard Mater 185, 970–976 (2011). (Diese Arbeit stellt einen geringen Bindungseffekt von Nitrat auch auf unbehandelten Klinoptilolith fest.)
[7] Xu, Y. H., Nakajima, T. & Ohki, A. Adsorption and removal of arsenic(V) from drinking water by aluminum-loaded Shirasu-zeolite. J Hazard Mater 92, 275–287 (2002).
[8] Bai, Y., Sun, Q., Sun, R., Wen, D. & Tang, X. Comparison of denitrifier communities in the biofilms of bioaugmented and non-augmented zeolite-biological aerated filters. Env. Technol 33, 1993–1998 (2012).
[9] Jiang, Y. F., Liu, D. H., Sun, T. X. & Chen, J. M. [Process characteristics of zeolite media biological aerated filter for treating aquaculture wastewater]. Huan Jing Ke Xue 31, 703–708 (2010).
[10] Eyde, T. H. Zeolites. Mining Engineering (2005).
[11] Nakamura, H. K., Ogawa, N., Uchida, S., Ochiai, T. & Takaoki, M. Water purification system by using the biofilter for long-term experiment equipment with aquatic animals for the space station. Life Support Biosph Sci 5, 353–356 (1998).
Schreibe einen Kommentar